
Debido a que la cultura de cualquier tipo no se vive en forma individual, sino grupal. Los valores son compartidos con los nuevos miembros de la compañía y puestos en práctica en los grupos a través de las normas y comportamientos (hábitos).
Este es el escenario que enfrentan hoy en día las Organizaciones, y que, de alguna manera, le dan un sello distintivo, dada la conducta de las personas que trabajan en ellas. Sin embargo, a veces esa característica o sello no es el deseado y escuchamos expresiones tales como “así se trabaja aquí”, “siempre lo hemos hecho así” o “¿para qué hay que cambiar esto o aquello si igual funciona?”, todo lo cual no hace más que dificultar el desarrollo y mejora continua que los estándares de Calidad e Inocuidad exigen hoy en día.
En la actualidad normativas tales como BRCGS versión 9 o FSSC 22000 versión 6, ya han incluido en sus requisitos el establecer, implementar y mantener objetivos relativos a una cultura de calidad e inocuidad, y que estos sean respaldados mediante un PLAN. Dicho plan debe tener un soporte y una razón de ser, que permitan realizar el debido seguimiento y medición respecto de las mejoras y la evolución en los cambios conductuales de las personas, lo cual es de gran interés para la Alta Gerencia.
Por esta razón, es que las Organizaciones deberían tomar en cuenta su razón de ser, es decir su Propósito (los Valores Corporativos, su Visión y Misión), las Personas, y herramientas tales como los Análisis de Peligros y enfoque de Riesgos. Cada uno de estos elementos puede perfectamente ser vinculado a los requisitos de las distintas normativas, por ejemplo:
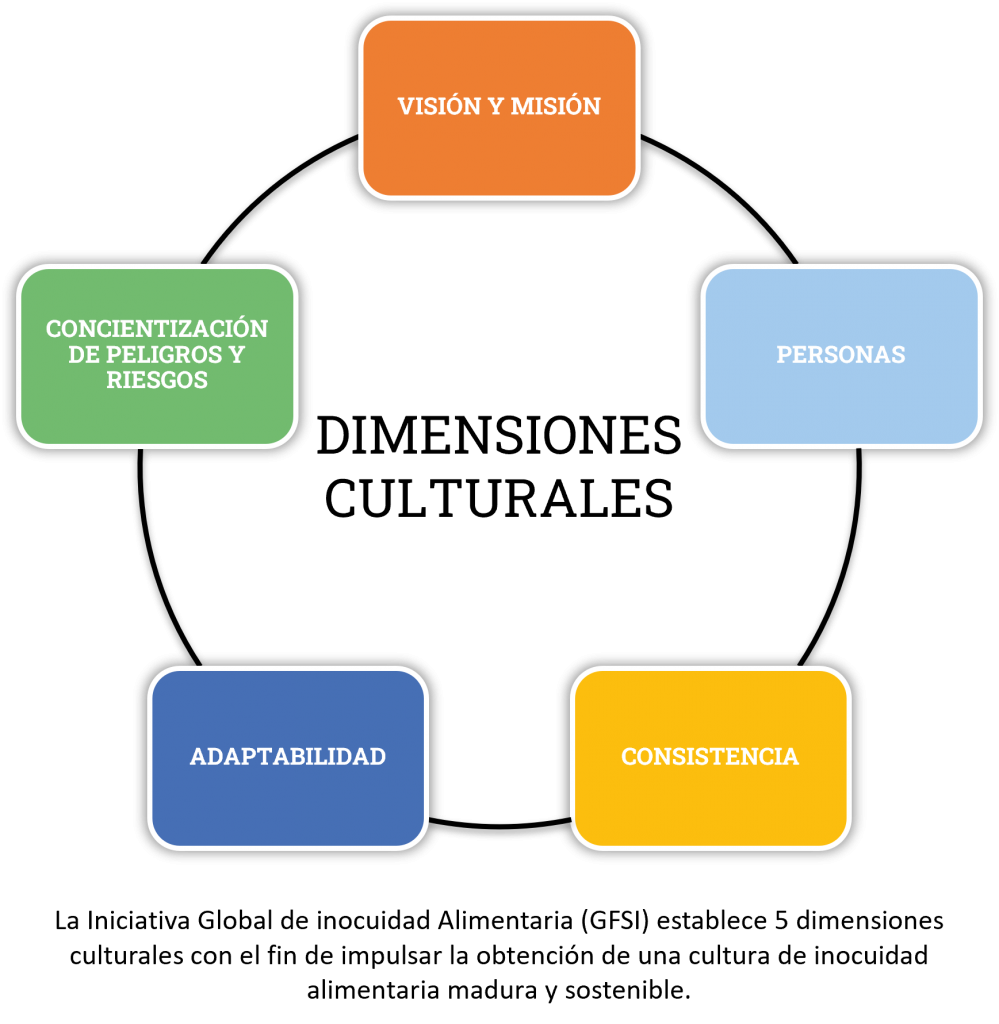
Es recomendable que, mediante un levantamiento inicial, la Organización conozca su grado de madurez respecto al Plan que desea implementar y así defina las dimensiones a desarrollar. Para esto se podría recopilar información que aborde aspectos tales como:

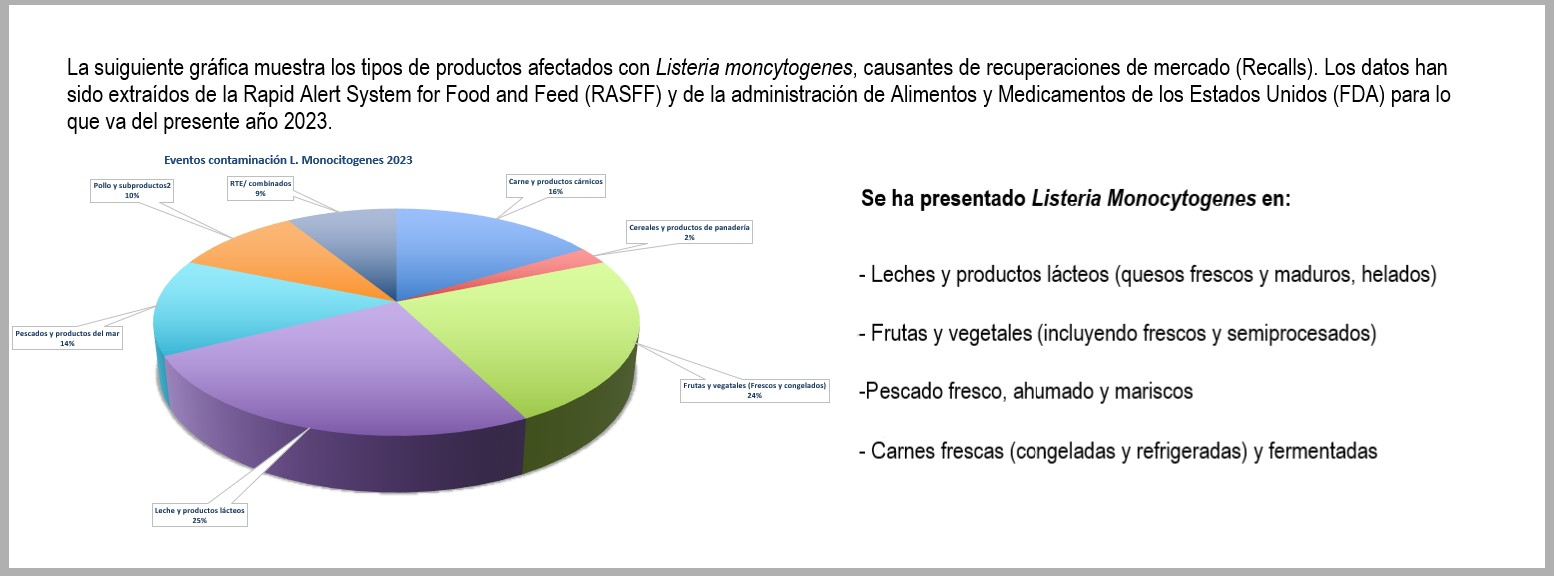
Una de las bacterias patógenas que se puede encontrar en los alimentos es la Listeria monocytogenes. Según datos del CDC durante el año 2022, se tiene un estimado de que 1.600 personas se enferman de listeriosis y cerca de 260 personas mueren anualmente, perjudicando especialmente a mujeres embarazadas y provocando abortos espontáneos. La infección por L. monocytogenes tiene dos formas de presentación de la enfermedad:
Corresponde a la forma leve de la enfermedad su periodo de incubación de la forma no invasiva generalmente es de 18 horas (11 horas a 7 días). Las consecuencias incluyen Fiebre, Diarrea, Dolores musculares, Náuseas, Vómitos, Somnolencia y Fatiga.
Corresponde a la presencia de L. monocytogenes en sangre y en el líquido cefalorraquídeo. Para el caso de la forma invasiva, el promedio es de 30 días (1 a 90 días), las consecuencias incluyen endocarditis, encefalitis, meningitis bacteriana, abortos y septicemias.
La Listeria monocytogenes se puede encontrar en ambientes húmedos, tierra, vegetación en descomposición; por lo que su ingreso al sector de proceso puede producirse por diferentes vías, mediante polvo exterior a la sala de proceso, si los exteriores no están adecuadamente pavimentados, o si en el entorno de procesamiento no se encuentra un diseño higiénico drenable y/o la utilización de aire comprimido en los procesos de aseo.
Este microorganismo es conocido por su resistencia a los procesos de erradicación debido a su capacidad de formar biofilms. Estos son una comunidad de microorganismos formada por una matriz de polisacáridos adherida a las superficies de procesamiento, el cual presenta una fase de maduración de 7-10 días para la dispersión y transferencia al ambiente, lo que podría resultar en producto potencialmente no inocuo (PPNI).
¿Quieres conocer si tu proceso de limpieza y desinfección es eficiente para su prevención?
¡Contáctanos!

 Santiago de Chile 29 de junio de 2022.
Santiago de Chile 29 de junio de 2022.

A través de la capacitación de usted puede cumplir con los requerimientos de la ley FSMA. Una de las regulaciones que forman parte de la ley FSMA requiere que aquellas compañías registradas con la FDA cuenten entre sus colaboradores con una persona calificada en controles preventivos (PCQI, por sus siglas en inglés).
Usted recibirá el certificado oficial de la IFPTI (International Food Protection Training Institute) al participar en nuestro seminario. Este es el único curso reconocido por la FDA para capacitar a una persona calificada en controles preventivos
«Es importante notar que es un requerimiento que todas
las empresas registradas con la FDA cuenten con una
persona calificada en controles preventivos (PCQI)». No
cumplir con esta regla limitará su habilidad para
exportar productos a los Estados Unidos.
Dirigido a:
Jefes, auditores e inspectores de aseguramiento de calidad e inocuidad alimentaria, que desarrollan la labor de realización del food safety plan, auditorias del plan y verificación de los controles preventivos de empresas que exportan alimentos a Estados Unidos, cubiertos por el reglamento de controles preventivos.
Agenda del curso:
Dia 1:
Dia 2:
Dia 3:
La Duración del Curso es de 24 horas (3 días)
Desde las 9:00 hrs. hasta las 18:00 hrs.
¡Ante cualquier consulta no dude en contactarnos mediante nuestros canales de comunicación!
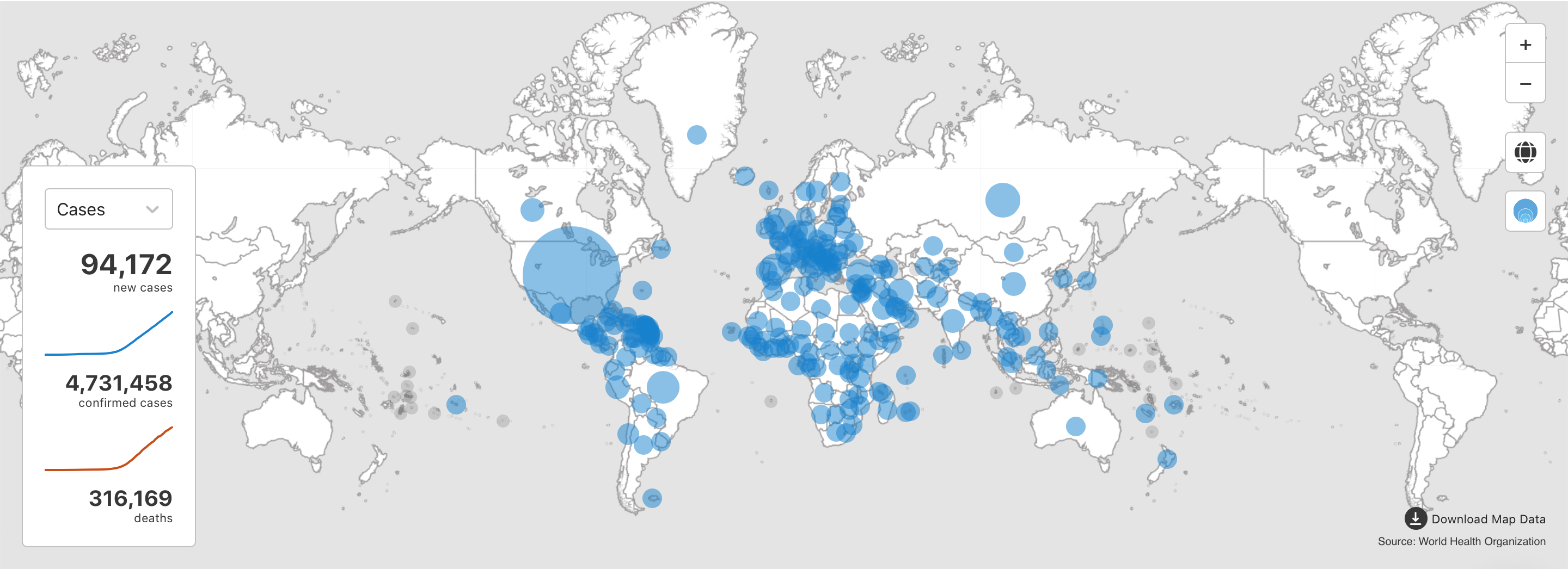
La Organización Mundial de la Salud, ha creado un sitio web en el que se muestra de forma estadística el avance de la enfermedad por país, continente o región.
En este sitio web se puede encontrar información oficial de la OMS acerca del actual brote de enfermedad por coronavirus (COVID-19) que fue notificado por primera vez en Wuhan (China) el 31 de diciembre de 2019. En esta página figura información actualizada diariamente.
La OMS está colaborando estrechamente con expertos mundiales, gobiernos y asociados para ampliar rápidamente los conocimientos científicos sobre este nuevo virus, rastrear su propagación y virulencia y asesorar a los países y las personas sobre la medidas para proteger la salud y prevenir la propagación del brote.
Fuente: OMS
Una vacuna contra el coronavirus parece haber proporcionado protección contra la enfermedad Covid-19 en seis monos macacos rhesus.
Da una esperanza temprana para la vacuna, que ahora se está sometiendo a ensayos clínicos en humanos. Sin embargo, no hay garantía de que este resultado se traduzca en personas.
Un grupo de monos fue expuesto al virus SARS-CoV-2. Los seis animales que fueron vacunados tenían menos virus en sus pulmones y vías respiratorias.
El ensayo tuvo lugar en los EE. UU., Con la participación de investigadores de los Institutos Nacionales de Salud (NIH) del gobierno de EE. UU. Y de la Universidad de Oxford. La vacuna parecía proteger a los animales contra el desarrollo de neumonía.
De manera prometedora, los animales tampoco desarrollaron una «enfermedad inmunoestimulada», que el corresponsal médico de la BBC Fergus Walsh describe como un «riesgo teórico». Es entonces cuando la vacuna desencadena una peor respuesta frente a una enfermedad.
Esta respuesta se observó en algunos de los primeros ensayos con vacunas animales contra el SARS, otro coronavirus, y demostró ser un impedimento en el desarrollo de una vacuna para esa enfermedad. El estudio aún no ha sido revisado por otros científicos ni ha sido publicado oficialmente, pero el profesor Stephen Evans, del London School of Hygiene and Tropical Medicine, lo describió como de «alta calidad» y «muy alentador». Mientras tanto, actualmente se llevan a cabo ensayos en el Reino Unido con más de 1,000 voluntarios humanos a través de la Universidad de Oxford. Actualmente se están desarrollando más de 100 vacunas experimentales de coronavirus.
Fuente: BBC: Coronavirus vaccine: Macaque monkey trial offers hope